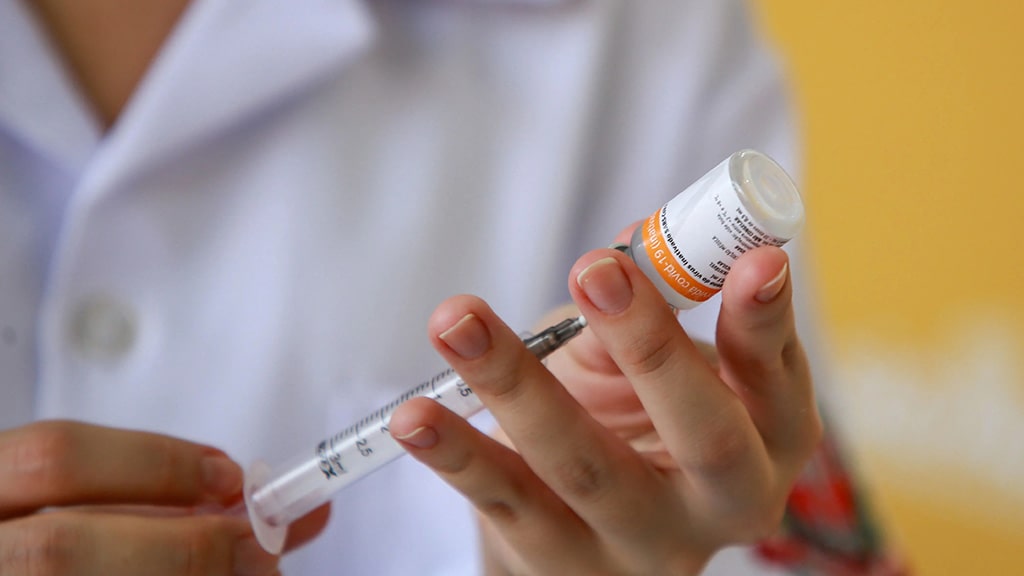
Vacinas e medicamentos – Norma publicada segunda-feira (5/6) permite uso dos produtos aprovados durante a pandemia.
A Anvisa publicou, nesta segunda-feira (5/6), a Resolução da Diretoria Colegiada (RDC) 801/2023, que permite a utilização dos medicamentos e vacinas que foram autorizados para uso emergencial durante a pandemia de Covid-19.
Leia também: Vacina brasileira contra vício em crack e cocaína concorre a prêmio internacional
Por que essa medida é necessária?
Com o fim da Emergência de Saúde Pública de Importância Nacional, a norma (RDC 688/2022) que estabelecia as regras para concessão e manutenção das Autorizações de Uso Emergencial (AUEs) perdeu a vigência.
Para que os medicamentos e vacinas aprovados por meio dessas autorizações ainda possam ser utilizados, a Anvisa publicou a nova norma, permitindo o uso, a distribuição e a comercialização desses produtos, desde que tenham sido fabricados até o último dia 21 de maio.

Vacinas e medicamentos
A norma publicada hoje reconhece que os medicamentos e vacinas mantêm sua eficácia e segurança e seguem com avaliação positiva na relação benefícios x riscos.
Quais são os medicamentos e vacinas aprovados para uso emergencial?
– Vacina Comirnaty bivalente BA.1.
– Vacina Comirnaty bivalente BA.4/BA.5.
– Vacina CoronaVac.
– Medicamento Sotrovimabe e Lagevrio (Molnupiravir).
– Medicamento Paxlovid (Nirmatrelvir + Ritonavir).
O que acontece agora?
Para continuarem a ser fabricados após 21 de maio, esses produtos precisam ter seu registro definitivo solicitado pelas empresas.
Até o momento, as vacinas CoronaVac e Comirnaty bivalente BA.4/BA.5, além do medicamento Paxlovid, já possuem pedido de registro em análise na Anvisa.